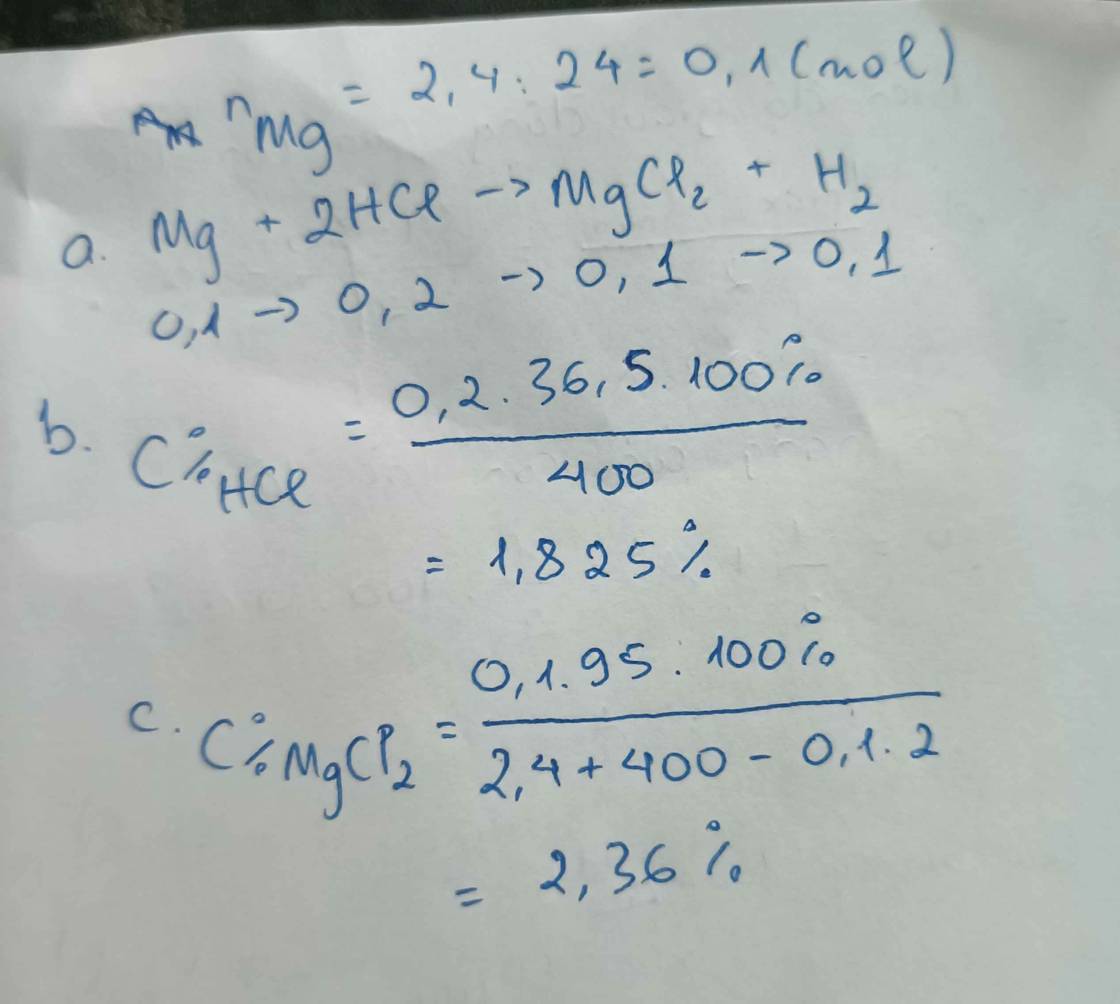cho 200 g dung dịch NAOH 10% phản ứng với 300 gam dung dịch HCL vừa đủ, tính nồng độ phần trăm của dung dịch sau phản ứng

Những câu hỏi liên quan
cho 200 gam dung dịch NaOH 20% tác dụng vừa hết với 100 g dung dịch HCl. Tính nồng độ phần trăm dung dịch muối sau phản ứng, tính nòng độ phần trăm dung dịch axit HCl đã dùng.Biết phản ứng xảy ra hoàn toàn
cho 11,2 gam sắt tác dụng vừa đủ với 200 gam dung dịch HCL. a) tính nồng độ phần trăm của dung dịch HCL. b) tính nồng độ phần trăm của dung dịch muối thu được sau phản ứng?
a) $n_{Fe} = \dfrac{11,2}{56} = 0,2(mol)$
$Fe + 2HCl \to FeCl_2 + H_2$
$n_{HCl} =2 n_{Fe} = 0,2.2 = 0,4(mol)$
$C\%_{HCl} = \dfrac{0,4.36,5}{200}.100\% = 7,3\%$
b) $n_{H_2} = n_{FeCl_2} = n_{Fe} = 0,2(mol)
Sau phản ứng, $m_{dd} = 11,2 + 200 - 0,2.2 = 210,8(gam)$
$C\%_{FeCl_2} = \dfrac{0,2.127}{210,8}.100\% = 12,05\%$
Đúng 2
Bình luận (0)
Bài 6: Cho 21,4 gam Fe(OH)3 tác dụng vừa đủ với 200 gam dung dịch Hydrochloric acid HCl. a) Tính nồng độ phần trăm của dung dịch HCl? b) Tính nồng độ phần trăm của dung dịch muối thu được sau phản ứng? Bài 7 : Cho m (g) Zinc oxide ZnO tác dụng vừa đủ 100g dung dịch Sulfuric acid H2SO4 9,8%. a) Tính m b) Tính C% dung dịch muối thu được.
Bài 6:
\(n_{Fe\left(OH\right)_3}=\dfrac{21,4}{107}=0,2\left(mol\right)\)
PT: \(Fe\left(OH\right)_3+3HCl\rightarrow FeCl_3+3H_2O\)
_______0,2________0,6______0,2 (mol)
a, \(C\%_{HCl}=\dfrac{0,6.36,5}{200}.100\%=10,95\%\)
b, \(C\%_{FeCl_3}=\dfrac{0,2.162,5}{21,4+200}.100\%\approx14,68\%\)
Đúng 2
Bình luận (0)
Bài 7:
\(m_{H_2SO_4}=100.9,8\%=9,8\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{9,8}{98}=0,1\left(mol\right)\)
PT: \(ZnO+H_2SO_4\rightarrow ZnSO_4+H_2O\)
______0,1______0,1_______0,1 (mol)
a, \(m_{ZnO}=0,1.81=8,1\left(g\right)\)
b, \(C\%_{ZnSO_4}=\dfrac{0,1.161}{8,1+100}.100\%\approx14,89\%\)
Đúng 1
Bình luận (0)
Cho 26 g Zn phản ứng vừa đủ với 150 g dung dịch HCl. Sau phản ứng thu được dung dịch muối kẽm và khí hiđro. A. Tính thể tích khí H2 thu được sau phản ứng (đktc). B. Tính nồng độ phần trăm dung dịch axit HCl đã dùng. C. Tính nồng độ phần trăm của dung dịch muối thu được sau phản ứng
\(n_{Zn}=\dfrac{26}{65}=0,4\left(mol\right)\\ pthh:Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
0,4 0,8 0,4 0,4
\(a,V_{H_2}=0,4.22,4=8,96\left(l\right)\\ b,C\%_{HCl}=\dfrac{0,8.36,5}{150}.100\%=19,5\%\\ c,m_{\text{dd}}=26+150-\left(0,4.2\right)=175,2\left(g\right)\\ C\%_{ZnCl_2}=\dfrac{0,4.136}{175,2}.100\%=31\%\)
Đúng 4
Bình luận (0)
Cho 75 gam dung dịch HCl 10,95% phản ứng vừa đủ với Fe2O3. Tính C% của chất tan trong dung dịch sau phản ứng?
Cho 10,2 gam Al2O3 vào 200 gam dung dịch HCl 14,6%. Tính nồng độ % của dung dịch muối sau phản ứng?
1.
\(m_{HCl}=\dfrac{10,95.75}{100}=8,2125\left(g\right)\)
\(\Rightarrow n_{HCl}=\dfrac{8,2125}{35,5}=0,225\left(mol\right)\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
\(\Rightarrow n_{Fe_2O_3}=\dfrac{1}{6}n_{HCl}=0,0375\left(mol\right)\)
\(n_{FeCl_3}=\dfrac{1}{3}n_{HCl}=0,075\left(mol\right)\)
\(\Rightarrow C\%=\dfrac{0,075.162,5}{0,0375.160+75}.100\%=15,05\%\)
Đúng 1
Bình luận (1)
2.
\(n_{Al_2O_3}=0,1\left(mol\right);n_{HCl}=0,8\left(mol\right)\)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
Dễ thấy HCl dư.
\(\Rightarrow n_{AlCl_3}=2n_{Al_2O_3}=0,2\left(mol\right)\)
\(\Rightarrow m_{AlCl_3}=26,7\left(g\right)\)
\(\Rightarrow C\%=\dfrac{26,7}{10,2+200}.100\%=12,7\%\)
Đúng 1
Bình luận (1)
5/ Cho 20,4 gam nhôm oxit phản ứng vừa đủ với 200 g dung dịch HCla. Tính thể tích khí sinh ra ( đktc)b. Tính khối lượng axit cần dùngc. Tính nồng độ phần trăm của dung dịch HCld. Tính nồng độ phần trăm của dung dịch sau phản ứnge. Nếu trung hòa lượng HCl trên bằng 100 g dung dịch NaOH 20 %, thì dung dịch sau phản ứng làm đổi màu quỳ tím như thế nào ?
Đọc tiếp
5/ Cho 20,4 gam nhôm oxit phản ứng vừa đủ với 200 g dung dịch HCl
a. Tính thể tích khí sinh ra ( đktc)
b. Tính khối lượng axit cần dùng
c. Tính nồng độ phần trăm của dung dịch HCl
d. Tính nồng độ phần trăm của dung dịch sau phản ứng
e. Nếu trung hòa lượng HCl trên bằng 100 g dung dịch NaOH 20 %, thì dung dịch sau phản ứng làm đổi màu quỳ tím như thế nào ?
\(a,n_{Al_2O_3}=\dfrac{20,4}{102}=0,2\left(mol\right)\\ PTHH:Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\\ .......0,2......1,2......0,4.....0,6\left(mol\right)\\ V_{H_2O\left(đktc\right)}=0,6\cdot22,4=13,44\left(l\right)\\ b,m_{HCl}=36,5\cdot1,2=43,8\left(g\right)\\ c,m_{dd_{HCl}}=1,2\cdot36,5=43,8\left(g\right)\\ C\%_{dd_{HCl}}=\dfrac{43,8}{200}\cdot100\%=21,9\%\)
\(d,m_{AlCl_3}=0,4\cdot133,5=53,4\left(g\right)\\ m_{dd\left(sau.pứ\right)}=m_{Al_2O_3}+m_{dd_{HCl}}-m_{H_2}=20,4+200-10,8=209,6\left(g\right)\\ C\%_{dd_{AlCl_3}}=\dfrac{53,4}{209,6}\cdot100\%\approx25,48\%\)
Đúng 2
Bình luận (1)
d)\(m_{NaOH}=\dfrac{mct.C\%}{100}=\dfrac{100.20}{100}=20\left(g\right)\)=>\(n_{NaOH}=\dfrac{20}{40}=0,5\left(mol\right)\)
\(HCl+NaOH\rightarrow NaCl+H_2O\)
tl1............1.............1..............1(mol)
So sánh\(\dfrac{n_{NaOH}}{1}< \dfrac{n_{HCl}}{1}\left(\dfrac{0,5}{1}< \dfrac{1,2}{1}\right)\)
=> HCl Dư
Vậy Dung dịch sau phản ứng làm quỳ tím chuyển màu đỏ
Đúng 2
Bình luận (0)
cho 2,4gam Mg phản ứng vừa đủ với 400gam dung dịch hcl.
a) viết pthh xảy ra
b) tính nồng độ phần trăm của dung dịch hcl đã dùng
c) tính nồng độ phần trăm của muối trong dung dịch sau phản ứng
a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
b, Ta có: \(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{Mg}=0,2\left(mol\right)\Rightarrow C\%_{HCl}=\dfrac{0,2.36,5}{400}.100\%=1,825\%\)
c, Theo PT: \(n_{MgCl_2}=n_{H_2}=n_{Mg}=0,1\left(mol\right)\)
Ta có: m dd sau pư = 2,4 + 400 - 0,1.2 = 402,2 (g)
\(\Rightarrow C\%_{MgCl_2}=\dfrac{0,1.95}{402,2}.100\%\approx2,36\%\)
Đúng 1
Bình luận (0)
Cho 13g Zn phản ứng vừa đủ với 150 g dung dịch HCl. Sau phản ứng thu được dung dịch muối và khí hiđro. A. Tính thể tích khí H2 thu được sau phản ứng (đktc). B. Tính nồng độ phần trăm của dung dịch HCl
`n_[Zn]=13/65=0,2(mol)`
`Zn + 2HCl -> ZnCl_2 + H_2 \uparrow`
`0,2` `0,4` `0,2` `(mol)`
`a)V_[H_2]=0,2.22,4=4,48(l)`
`b)C%_[HCl]=[0,4.36,5]/150 .100~~9,73%`
Đúng 8
Bình luận (7)
Cho Mg phản ứng vừa đủ với 300 gam dung dịch HCl 7,3%
a. Tính khối lượng Mg phản ứng.
b. Tính nồng độ % của dung dịch MgCl2 thu được sau phản ứng.
Ta có: \(m_{HCl}=300.7,3\%=21,9\left(g\right)\Rightarrow n_{HCl}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
___0,3_____0,6_____0,3____0,3 (mol)
a, mMg = 0,3.24 = 7,2 (g)
b, Ta có: m dd sau pư = mMg + m dd HCl - mH2 = 7,2 + 300 - 0,3.2 = 306,6 (g)
\(\Rightarrow C\%_{MgCl_2}=\dfrac{0,3.95}{306,6}.100\%\approx9,3\%\)
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
pthh:Mg+2HCl→MgCl2+H2(1)
theo pthh=>\(nMg=\dfrac{1}{2}nHCL=\dfrac{300.7,3\%}{7,3}.\dfrac{1}{2}=\dfrac{3.1}{2}=1,5mol\)
=>mMg=\(1,5.24=36g\)
b, theo pthh(1)\(=>nMgCl2=\dfrac{1}{2}nHCL=1,5mol\)
\(=>mMgCl2=\)\(1,5.95=142,5g\)
\(mdd=\text{ m Mg + mdd HCl - m H2}=36+300-1,5.2=333g\)
\(=>\%mMgCl2=\dfrac{142,5}{333}.100\%=42,8\%\)
Đúng 0
Bình luận (1)
: Cho 10 gam CaCO3 phản ứng vừa đủ với 200 gam dung dịch HNO3, phản ứng tạo Ca(NO3)2 (tan), khí CO2 và nước.
a/ Tính nồng độ % của dung dịch HNO3.
b/ Tính nồng độ % của dung dịch thu được sau phản ứng.
\(n_{CaCO_3}=\dfrac{10}{100}=0,1\left(mol\right)\)
a.
\(CaCO_3+2HNO_3\rightarrow Ca\left(NO_3\right)_2+H_2O+CO_2\)
0,1 0,2 0,1 0,1
\(C\%_{dd.HNO_3}=\dfrac{0,2.63.100}{200}=6,3\%\)
b.
\(m_{dd.Ca\left(NO_3\right)_2}=10+200-0,1.44=205,6\left(g\right)\)
\(C\%_{dd.Ca\left(NO_3\right)_2}=\dfrac{0,1.164.100}{205,6}=7,98\%\)
Đúng 1
Bình luận (0)